Mehr als neun Millionen Menschen
erkranken jährlich weltweit neu an
einer Tuberkulose (TB); 1,5 Millio
nen von ihnen sterben daran. Er
schwert wird die Therapie dadurch,
dass sich Antibiotikaresistente Er
regerStämme ausbreiten.
Das Klinische Tuberkulosezent
rum des Deutschen Zentrums für
Infektionsforschung (DZIF) am
Forschungszentrum Borstel gehört
weltweit zu den führenden medizi
nischen Einrichtungen für die
Grundlagenforschung und die klini
sche Anwendung von Tuberkulosta
tika. Vor allem ist man auch auf die
Behandlung multiresistenter Tuber
kulosen (MDRTB) spezialisiert.
„Wir setzen zunehmend auf maßge
schneiderte Behandlungskonzepte,
bei denen die Antibiotika individu
ell zusammengestellt werden“, er
klärt Professor Christoph Lange,
Ärztlicher Leiter der Klinischen In
fektiologie in Borstel in einer Mit
teilung des Zentrums.
Den aktuellen Stand der Tuber
kulosetherapie haben die Forscher
nun im „New England Journal of
Medicine“ publiziert (NEJM 2015;
372: 2149). In einer interaktiven
Grafik können Ärzte weltweit für
unterschiedliche Behandlungssitua
tionen eine geeignete Therapie fin
den. Daneben bietet ein Ärzte
Team um Lange einen klinischen
Beratungsservice für Fragen zu TB
und Erkrankungen durch nicht
tuberkulöse Mykobakterien an. Für
die Beratung von Ärzten zur Thera
pie von Patienten mit multiresisten
ter TB haben sie mit Mitteln des
DZIF ein nationales TBOnline
Consilium aufgebaut.
(eb/eis)
Beratungsservice zu TB und anderen
Infektionen durch Mykobakterien unter
Tel.: 04537 / 188 2110. Nationales
TBOnlineConsilium unter
Consilium für
die Therapie der
Tuberkulose
Das Forschungszentrum
Borstel berät Ärzte zur
Therapie von Patienten
mit multiresistenter TB.
ONLINE
Die deutsche Version der Leitlinie
des European Resuscitation Coun
cil (ERC) 2015 ist in der Zeitschrift
„Notfall + Rettungsmedizin“ sowie
im Internet auf
ver
öffentlicht. In der neuen Leitlinie
werden Strategien zu mehr ausge
bildeten Ersthelfern, für intelligente
Alarmierungssysteme und für eine
deutliche Zunahme der Reanimati
onen durch Laien angeregt. The
men sind unter anderem
Basismaßnahmen und erweiterte
Maßnahmen zur Wiederbelebung
Erwachsener und Kinder,
Kreislaufstillstand unter beson
derern Umständen,
Initiales Management des akuten
Koronarsyndroms,
Ausbildung und Implementie
rung der Reanimation.
(eb)
Ausgaben der „Notfall + Rettungsme
dizin“ können bestellt werden über
Reanimation:
ERCLeitlinien
aktualisiert
NOTFALLMEDIZIN
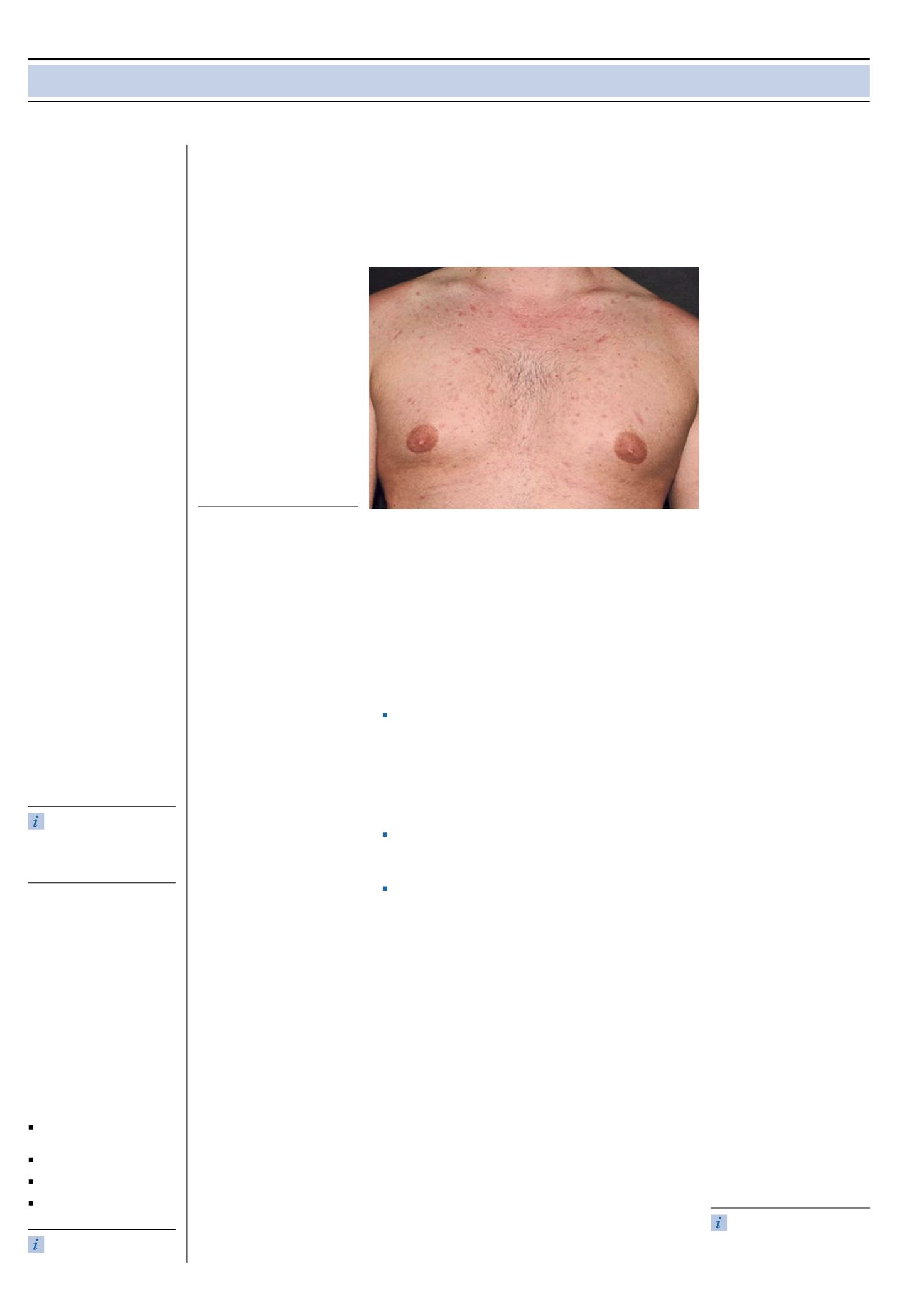
Ein 24jähriger männlicher Patient
stellte sich in unserer Notaufnahme
vor. Er berichtete über einen seit vier
Tagen bestehenden generalisierten
Hautausschlag (siehe Abbildung). An
welcher Stelle der Ausschlag begonnen
habe, könne er nicht mehr sagen. Be
reits seit sechs Tagen leide er unter
Appetitlosigkeit, habe Übelkeit und
Schüttelfrost. Zusätzlich habe er seit
zwei Tagen Durchfälle. Seit heute
klagte er außerdem über Halsschmer
zen, Husten und Gliederschmerzen.
Brennen beim Wasserlassen wurde
verneint.
Der Patient war Nichtraucher, lebte
noch bei seinen Eltern und befand
sich in einer kaufmännischen Ausbil
dung. Enge Kontaktpersonen wiesen
keine ähnlichen Symptome auf. Eine
feste Partnerschaft, Promiskuität,
homosexuelle Kontakte und ein Kon
sum illegaler Drogen verneinte der Pa
tient.
Befunde
Bei der körperlichen Untersuchung in
der zentralen Notaufnahme zeigten
sich ein generalisiertes, morbilliformes,
makulopapulöses Exanthem sowie ein
Enanthem am weichen Gaumen.
Lymphknoten an Kopf/Hals, axillär
und inguinal waren nicht vergrößert
palpabel. Periphere Ödeme fanden
sich nicht. Die Auskultation von Herz
und Lunge war unauffällig. Im Auf
nahmelabor fanden sich ein erhöhtes
Creatinin von 124 mol/l (
,
103
mol/l), eine verminderte GFR von
69 ml/min (80–140 ml/min), eine er
höhte GOT von 148 U/l (
,
40 U/l), ei
ne erhöhte GPT von 46 U/l (
,
41 U/l),
eine Leukopenie von 4,4 G/l (4,5–11,0
G/l) und eine Thrombopenie von 96
G/l (150–400 G/l). In der Lymphkno
tensonographie fielen axillär und in
guinal beidseits kokardenförmig ver
größerte Lymphknoten auf. In der Ab
domensonographie fand sich eine
leicht vergrößerte Milz mit 12 cm im
Längsdurchmesser. Die Röntgenun
tersuchung des Thorax war unauffäl
lig.
Der Patient wurde unter der Ar
beitsdiagnose „Virusexanthem“ zur
weiteren Durchuntersuchung stationär
aufgenommen.
Zum Ausschluss einer HIVirusIn
fektion führten wir während eines sta
tionären Aufenthalts einen HIV1/2
Antikörper/p24AntigenSuchtest
(Elecsys
®
HIV combi PT) durch. Auf
grund eines reaktiven Befundes erfolg
te am Folgetag eine Testwiederholung
mit einer erneuten Blutprobe. Bei wie
derholter Reaktivität erfolgte zur Absi
cherung der Diagnose die Durchfüh
rung eines LineImmunoassays (IN
NOLIATM HIV I/II Score). Dieser
fiel negativ aus. Auf Grundlage des kli
nischen Bildes und des reaktiven
HIVSuchtests führten wir unter der
Verdachtsdiagnose eines akuten retro
viralen Syndroms eine HIVRNA
PCR („polymerasechainreaction“)
durch, die mit
.
800000 Kopien hoch
positiv ausfiel und somit die Ver
dachtsdiagnose bestätigte.
Im ergänzenden Labor waren die
CD4Zellen normwertig mit 744 Zel
len pro l. Der CD4/8Quotient be
trug 1,82. Als Begleitinfektion fand
sich eine akute Zytomegalievirus
(CMV)Infektion. Die Verdachtsdiag
nose akutes retrovirales Syndrom wur
de somit bestätigt.
Therapie und Verlauf
Eine antiretrovirale Therapie mit Efa
virenz und Lamivudine/Zidovudine
wurde zeitnah eingeleitet. Bereits 92
Tage nach Therapiebeginn fiel die
Viruslast unter die Nachweisgrenze.
Der Infektionsweg blieb aufgrund
mangelnder Mitarbeit des Patienten
unklar.
Diskussion
HIV Typ I, erstmalig 1983 von Fran
çoise BarréSinoussi und Luc Montag
nier beschrieben, ist auch heute noch
mit 2954 Erstdiagnosen (2012) in
Deutschland ein hochaktuelles The
ma.
Untersuchungen an Patienten mit
früher HIV1Infektion haben gezeigt,
dass die Zeit bis zur HIVSerokonver
sion in verschiedene Phasen eingeteilt
werden kann. Fiebig und Kollegen de
finierten sechs Phasen auf der Grund
lage der zeitlichen Aufeinanderfolge,
wann welches HIVNachweisverfahren
anspricht. Hierbei entspricht die Ec
lipse der Zeit, in der eine HIVInfekti
on nicht nachgewiesen werden kann.
In Phase I kann HIVRNA mittels
PCR nachgewiesen werden. In Phase
II besteht zusätzlich die Möglichkeit,
das p24Antigen mittels ELISA nach
zuweisen. In Phase III werden Anti
körpersuchtests (ELISA) ebenfalls po
sitiv. Das Auftreten der Antikörper er
schwert hierbei die p24Detektion. Ab
Phase IV wird der WesternBlot indif
ferent, ab Phase V positiv. In Phase VI
ist der WesternBlot vollständig ausge
bildet, p31 ist nun ebenfalls nachweis
bar.
Auf Basis dieser Chronologie wird
heute zur Testung zunächst die
Durchführung sogenannter Viertgene
rationssuchtests empfohlen. Diese
Testsysteme sind in der Lage, neben
den HIV1 und 2Antikörpern auch
das bereits früher nachweisbare p24
Antigen nachzuweisen. Hierdurch ist
es möglich, die „diagnostische Lücke“
um sieben bis elf Tage zu verkürzen.
Da diese Testsysteme hochsensitiv
sind, ist es notwendig, bei reaktivem
Ausfall das Ergebnis durch hochspezi
fische Testsysteme, zum Beispiel dem
WesternBlot oder dem LineImmu
noassay, zu bestätigen.
Herausforderung in der Diagnostik
Im Rahmen dieser Diagnostik stellt
das akute retrovirale Syndrom eine be
sondere Herausforderung dar. Unter
diesem versteht man die symptomati
sche Phase der HIVErstinfektion, die
allerdings nur bei einigen Infizierten
auftritt und selten länger als vier Wo
chen andauert. Die Symptome sind
eher unspezifisch und variabel. Leit
symptome sind Fieber, Lymphknoten
schwellung, makulopapulöses Exan
them und Myalgien. Spezifische Anti
körper sind noch nicht nachweisbar,
da die spezifische Immunantwort ver
zögert einsetzt und spezifische Anti
körper erst im Verlauf produziert wer
den. Somit fallen oben genannte Test
systeme in Hinblick auf den Antikör
pernachweis negativ aus, obwohl eine
Infektion mit dem HIVirus vorliegt.
Hinzu kommt, dass zu diesem Zeit
punkt die Viruslast im Blut und in Ge
nitalsekreten höher ist als im weiteren
Verlauf. Dadurch bedingt ist die Infek
tiosität während dieser Phase beson
ders hoch. Erst im weiteren Verlauf
nimmt sie durch das Einsetzen der
spezifischen Immunantwort wieder ab.
Aus diesem Grund gehen einige Auto
ren davon aus, dass ein Großteil der
sexuellen Transmissionen durch Pati
enten, die sich in dieser Frühphase der
Erkrankung befinden, verursacht wer
den.
Daher sollte bei Patienten mit
unspezifischen Zeichen einer akuten
Virusinfektion zumindest an die Mög
lichkeit einer akuten HIVirusInfekti
on gedacht und eine entsprechende
Anamnese zur Risikoabschätzung
durchgeführt werden. Sollte es Hin
weise für das Vorliegen eines akuten
retroviralen Syndroms geben, ist die
Durchführung einer HIVPCR sinn
voll, um die Diagnose zu sichern, den
frühzeitigen Beginn einer antiretrovira
len Therapie zu diskutieren und letzt
endlich die Transmissionsraten effektiv
zu senken.
Der Nutzen eines frühzeitigen
Beginns der antiretroviralen Therapie
während der akuten HIVInfektion
wird derzeit kontrovers diskutiert. Als
Nachteile werden unter anderem
Medikamententoxizität und Resistenz
entwicklung aufgeführt. Aus unserer
Sicht ist der frühe Beginn jedoch
durchaus sinnvoll – zum einen um die
Viruslast und damit den viralen
Setpoint zu senken und zum anderen
zur Verringerung des Transmissions
risikos während der Phase höchster In
fektiosität.
Auch die Frage nach der Dauer der
antiretroviralen Therapie beziehungs
weise nach Therapieunterbrechungen
wird kontrovers diskutiert. Therapie
pausen sind nach den Ergebnissen der
SMARTStudie als obsolet anzusehen.
Sollte jedoch ein dringlicher Patien
tenwunsch nach einer Therapiepause
bestehen, so ist es besser, eine kontrol
lierte Pause durchzuführen und gege
benenfalls frühzeitig wieder mit einer
antiretroviralen Therapie zu beginnen.
Dieser Beitrag von Dr. René Stranzenbach
und Professor Rudolf Stadler vom
Johannes Wesling Klinikum Minden wurde
bereits in der Zeitschrift Der Hautarzt
2015; 66: 282284 veröffentlicht.
Zu Beginn eines akuten
retroviralen Syndroms hat
die spezifische Antikörper
antwort noch nicht einge
setzt, sodass auf Antikörper
basierende HIVSuchtests
negativ ausfallen. Das ist
problematisch, da in dieser
Phase die Viruslast massiv
höher ist als im weiteren
Verlauf. Damit ist auch die
Infektiosität des Patienten
um ein Vielfaches erhöht.
Akutes retrovirales Syndrom:
Diagnostische Lücke verkürzen!
Von Dr. René Stranzenbach und
Professor Rudolf Stadler
Generalisiertes, morbilliformes, makulopapulöses Exanthem.
© SPRINGER VERLAG GMBH
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
Fazit für die Praxis
Bei Patienten
mit Zeichen eines
unklaren viralen Infektes (Fieber,
Lymphknotenschwellung, maku
lopapulöses Exanthem, Myal
gien) und positiver Risikoanam
nese sollte im Rahmen der diffe
renzialdiagnostischen Überle
gungen an die Möglichkeit einer
akuten HIVInfektion gedacht
werden.
Bei unklarer Konstellation
sollte die Durchführung einer
HIVRNAPCR zur frühzeitigen
Diagnosesicherung erfolgen.
Der frühzeitige Beginn
einer
antiretroviralen Therapie ist
anzustreben.
14
Januar 2016
BDI aktuell
Medizin


