Medizin
BDI aktuell
Juni 2016
15
Wir berichten von einer 39jährigen,
asylsuchenden syrischen Patientin, die
uns zur Abklärung pulmonaler und
kutaner Veränderungen im März 2014
eingewiesen wurde. 3,5 Jahre vorher
erlitt sie nach einer fraglichen Giftgas
exposition in Homs eine langsam zu
nehmende Dyspnoe. Zusätzlich waren
Hautveränderungen sichtbar, welche
sich mit entzündlichen, plattenartigen
zum Teil akneiformen Veränderungen
manifestierten. Die primäre Vorstel
lung erfolgte in der Dermatologie und
anschließend in der Pneumologie we
gen zunehmender respiratorischer In
suffizienz bei ausgeprägten zystischen
Veränderungen in beiden Lungen. Die
Patientin ist Nieraucherin und Mutter
von drei gesunden Kindern. In Syrien
wurde die Patientin bereits wegen
eines Pneumothorax operiert. Anfang
2014 kam sie nach Deutschland. Die
Familienanamnese im Hinblick auf
pulmonale und dermatologische Er
krankungen ist leer.
Klinischer Befund
Die Patientin befand sich in einem re
duzierten Allgemeinzustand und un
auffälligen Ernährungszustand. Sie
war tachypnoisch. Am Kopf waren
scharf begrenzte plattenartig indurier
te entzündliche Hautveränderungen
zu erkennen (siehe Abbildung). Inner
halb dieser bis zu 10 cm durchmessen
den Plaques manifestierten sich neben
Pusteln vereinzelt auch eitrige ulzerie
rende Knoten an der frontalen Halsre
gion, am Unterbauch und in der Geni
talregion. Keine Ödeme. Pulmohyper
sonorer Klopfschall beidseits und aus
kultatorisch abgeschwächtes Atemge
räusch, Herztöne rein und rhythmisch,
Bauch weich, kein Druckschmerz. Ori
entierende neurologische Untersu
chung unauffällig.
Diagnostik
Routinelabor: Unauffällig, Alpha
1Antitrypsin normal.
BGA vom 18.03.2014 unter Raum
luft: pH 7,47, pO
2
56 mmHg, pCO
2
33 mmHg, Sauerstoffsättigung 91%,
schwere Hypoxämie.
BGA mit 4 l Sauerstoff/Minute
02.07.2015: pH 7,49, pCO
2
37,0
mmHg, pO
2
70,4 mmHg, Sauerstoff
sättigung 93,7%.
Bodyplethysmographie: In der Lun
genfunktion liegt spirometrisch keine
Obstruktion vor. Es zeigt sich eine re
lative Lungenüberblähung (FEV1 1,15
l (46,1%), VC 1,44 l (45,4%),
FEV1/VC 86,12%, TLC 4,43 l
(95,5%)). Die Diffusionskapazität
(TLCOcSB) ist mit 17,3% stark ein
geschränkt.
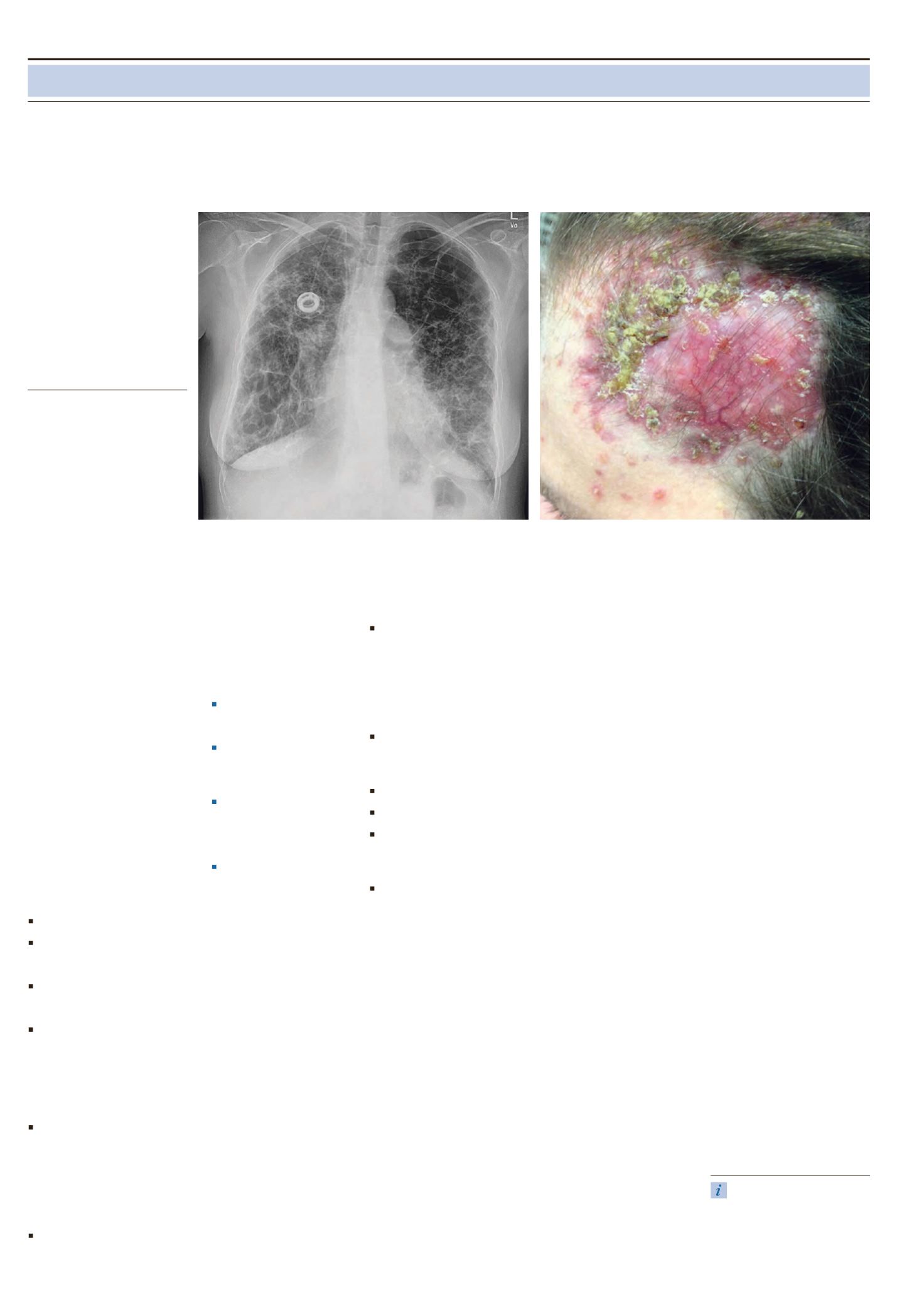
Röntgenthorax: Ausgeprägte fibroti
sche Veränderungen der Lungenmit
telund unterfelder beidseits sowie
der Oberfelder rechts mehr als links.
Weitere bullös emphysematische Ver
änderungen auch in den übrigen Lun
genabschnitten. Normale Herzgröße.
Pulmonalissegment prominent.
Schmales u. mittelständiges oberes
Mediastinum (siehe Abbildung).
CTThorax: Hochgradiger panlobu
lärer Emphysemaspekt mit multiplen
bullösen Veränderungen. Kein Pneu
mothorax oder Pleuraerguss. Kein In
filtrat erkennbar. Im Knochenfenster
keine metastasenverdächtigen Verän
derungen. Altersentsprechende ossäre
Strukturen.
Flexible Bronchoskopie: Im Oro
pharynx und Nasenbereich bds. ent
zündlich kontaktvulnerable Schleim
haut. Die Kehlkopfregion unauffällig,
dichter Stimmlippenschluss. Im ge
samten Bronchialsystem bds. diffuse
leichtgradige Hämorrhagien. Nach
Absaugung freie Sicht in alle Segmen
te, kein zentraler Tumor sichtbar, kei
ne Sekretretention.
Bronchoalveoläre Lavage: Lympho
zyten 13%, Alveolarmakrophagen
60%; Neutrophile 24%, Eosinophile
3%; CD4/CD8 0.97; CD1apositive
Zellen 4%.
Bakteriologie: Vergrünende Strepto
kokken.
Tuberkulose: Mikroskopisch und
kulturell negativ.
Hautbiopsie: Entnahme von 2
Hautproben mittels Biopsie vom be
haarten Kopf sowie vom Mons pubis
in Lokalanästhesie mit primärem
Wundverschluss.
Histologie: In Zusammenschau der
konventionell histologischen und im
munhistochemischen Befunde handelt
es sich um eine lymphoplasmazellulä
re, ulzerierende und hier auch mit
Granulozyten versehene Entzündungs
reaktion der Dermis im Bereich des
Kopfes und des Mons pubis. Keine
Anteile einer epithelialen Neoplasie.
Keine klassische Granulomatose. Kein
Anhalt für Malignität. Die Hautbiop
sie ergab ein dichtes Infiltrat histiozy
tärer Zellen, daneben Plasmazellen
und Eosinophile sowie die histiozytä
ren Zellen exprimieren CD1a und
S100 und Langerin.
Verlauf
Nach Aufnahme der Patientin konnte
in Zusammenschau von klinischen Be
funden, Bildgebung, Histologie und
Immunhistologie eine Langerhans
ZellHistiozytose gesichert werden,
welche sich in der Lunge, an der Haut
und den Knochen manifestierte. An
fänglich zeigte sich eine schwere noch
nicht sauerstoffpflichtige respiratori
sche Insuffizienz, die sich aber weiter
verschlechterte und eine Sauerstoff
therapie notwendig machte.
Zur Behandlung der Langerhans
ZellHistiozytose leiteten wir gemein
sam mit der Evangelischen Lungenkli
nik BerlinBuch eine Therapie mit
Prednisolon 60 mg Tag 15 und Vin
blastin (3,7 mg/m
2
) als Bolus aller 3
Wochen ein. Die dermatologischen
Manifestationen zeigen eine deutliche
Besserung, während die pulmonalen
Veränderungen sich erwartungsgemäß
irreversibel zeigen. Bei zunehmender
Sauerstoffpflichtigkeit wird Lungen
transplantation erwogen. Begleiter
krankungen oder schwere Nebenwir
kungen sind nicht zu verzeichnen.
Diskussion
Die Erstbeschreibung der Langer
hansZellHistiozytose erfolgte 1868
durch Paul Langerhans. Er vermutete
bei Hautveränderungen aufgrund der
dendritischen Gestalt dieser Zellen,
dass es sich um intraepidermale Ner
venzellen handelt, und interpretiert sie
als das anatomische Substrat der Be
rührungsempfindung. Die Langer
hansZellHistiozytose (LCH) ist eine
seltene Erkrankung, bei Erwachsenen
wird ihre Inzidenz auf mindestens
1015 pro 1000000 pro Jahr ge
schätzt. Sie tritt am häufigsten bei
Kindern zwischen 1 und 15 Jahren auf
vorwiegend mit einem disseminierten
Befall der inneren Organe und des
ZNS. Bei Erwachsenen ist ein isolier
ter pulmonaler Befall am häufigsten.
Die Histiozytose X kann man in eine
monosystemische LCH (single sys
tem disease) und eine multisystemi
sche LCH (multisystem disease)
unterscheiden. Je nach der Anzahl be
fallener Organe und Einzelorganbetei
ligung spricht man von einer uniloku
lären oder von einer multilokuären Er
krankung. 50 Prozent der Erkrankun
gen treten bis zum 10. Lebensjahr auf
und 75 Prozent bis zum 30. Lebens
jahr. Bei unserer Patientin liegt eine
seltene multisystemische LCH mit
pulmonalem Befall, Haut und ossärer
Beteiligung bei einer 38jährigen Pati
entin vor. Die LCH tritt praktisch nie
bei Nichtrauchern auf, ein Passivrau
chen liegt bei ihr vor, der Giftgasan
griff bleibt spekulativ.
Zur Diagnosesicherung ist die Bi
opsie mit histopathologischer bzw. im
munhistochemischer Untersuchung
von befallenem Gewebe unerlässlich.
Die definitive Diagnose einer LCH be
ruht neben Charakteristika in der kon
ventionellen Lichtmikroskopie auf
dem immunhistochemischen Nach
weis von CD1a Antigen und/oder
Langerin (CD207) auf der Zellober
fläche. Da der immunhistochemische
Nachweis von Langerin mit dem elekt
ronenmikroskopischen Nachweis von
BierbeckGranula korreliert, kann auf
die Elektronenmikroskopie verzichtet
werden. Zudem kann eine bronchoal
veoläre Lavage mit dem Nachweis von
4% CD1positiven Zellen die Diag
nose festigen. Wir konnten in unserem
Fall die Diagnose histologisch über
den immunhistochemischen Nachweis
von histiozytären Zellen bestätigen, die
kräftig S100Protein, CD1a und
Langerin (CD207) exprimieren. Zu
sätzlich fand sich in der BAL (Bron
choalveoläre Lavage) ein Nachweis
von 4% CD1apositiven Zellen.
Der Therapie und die Prognose
hängen von der Einordnung und dem
Ausmaß der Manifestation ab. Eine
ungünstige Prognose besteht im ju
gendlichen Alter bei ausgedehntem
Organbefall und geht einher mit des
sen Grad der Dysfunktion. Ein inter
disziplinärer Therapieansatz sollte er
folgen. Neben einer lokalen Therapie
sind systemische Therapieansätze not
wendig mittels Zytostatika wie 2Chlo
rodeoxyadenosin allein oder in Kom
bination mit Cytosinarabinosid sowie
der immunmodulatorischen Substanz
Thalidomid. Eine risikoadaptierte Po
lychemotherapie über ein Jahr kann
mit Vinblastin oder Etoposid in Kom
bination mit Prednisolon erfolgen. Bei
Knochenbefall ist auch eine Bispho
sponattherapie indiziert. Der Nach
weis einer Mutation der mitogenac
tivated protein kinase (MAPK) er
laubt eine TargetTherapie mit BRAF
oder MAP2K1Inhibitoren.
Aufgrund des Allgemeinzustandes
der Patientin und des Risikos der The
rapietoxizität haben wir uns für eine
Behandlung mit Vinblastin und Pred
nisolon mit bisher gutem Erfolg im
Hautbereich entschieden. Eine Besse
rung der Lungenbeteiligung war und
wird unter der Therapie nicht zu er
warten sein und eine Lungentrans
plantation wird erwogen. Die pulmo
nale Situation beeinflusst die Prognose
und wird entscheidend für den Verlauf
der Erkrankung. Da eine stabile klini
sche Situation über 1 Jahr vorliegt, ist
eine TargetTherapie in diesem Fall
noch nicht in Erwägung gezogen wor
den, vorher ist eine Bestimmung von
MAPK vorzunehmen.
Dieser Beitrag von Sadek AlDoghaishi,
Dr. Konrad Wetzer, Dr. LutzUwe Wölfer
und Frank Dietrich vom Lausitzer Seeland
klinikum Hoyerswerda sowie· Dr. Christian
Grohé von der Evangelischen Lungenklinik
BerlinBuch wurde bereits veröffentlicht in
Der Pneumologe 2016; 13: 120123.
Literatur bei den Autoren
War Giftgas Ursache für die Symptome?
Eine 39jährige NieRauche
rin wurde mit Zystenlunge,
Hautveränderungen und
Osteolysen eingewiesen. Seit
einer fraglichen Giftgasexpo
sition 3,5 Jahre zuvor, litt
sie an langsam zunehmender
Dyspnoe. Was war Ursache
der Beschwerden?
Von Sadek AlDoghaishi und Kollegen
Röntgenthorax.
© SPRINGER VERLAG GMBH
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
●
LangerhansZell
Histiozytose (LCH)
Die Inzidenz
der LCH wird auf
mindestens 1015 pro 1000000
pro Jahr geschätzt.
50 Prozent der Erkrankungen
treten bis zum 10. Lebensjahr
auf und 75 Prozent bis zum
30. Lebensjahr.
Zur Diagnosesicherung
ist die
Biopsie mit histopathologischer
bzw. immunhistochemischer
Untersuchung von befallenem
Gewebe unerlässlich.
Der Therapie und die Prognose
hängen von der Einordnung und
dem Ausmaß der Manifestation
ab.
Scharfbegrenzte plattenartig indurierte entzündliche Hautveränderungen (bis zu 10 cm)
auf dem Kopf der Patientin.
© SPRINGER VERLAG GMBH


